2025年医疗人工智能发展现状
文章目录
- 2025年医疗人工智能发展现状
- 一、医疗AI市场规模与增长趋势
- 全球市场概况
- 市场规模:整体扩张与细分赛道分化
- 增长速率:整体高增与细分市场差异显著
- 区域格局:北美主导与亚太崛起的双极态势
- 中国市场特点
- 二、技术进展与创新突破
- 核心技术演进
- 算法与算力支撑
- 三、应用场景与临床实践
- 临床诊疗核心场景
- 公共卫生与基层医疗
- 特殊领域创新应用
- 四、政策法规与监管环境
- 中国政策框架
- 国际监管比较
- 五、产业格局与企业竞争
- 中国市场主体
- 国际企业与跨国合作
- 六、挑战、伦理与风险
- 技术与数据挑战
- 伦理与监管风险
- 商业化与可持续性
- 七、患者接受度与社会影响
- 患者态度与使用行为
- 医疗资源普惠与社会公平
- 八、未来趋势与展望
- 技术融合与创新方向
- 政策与产业生态演进
- 商业化路径探索
2025年医疗人工智能发展现状
一、医疗AI市场规模与增长趋势
全球市场概况
全球医疗人工智能市场呈现高速扩张态势,本文采用“规模-增速-区域”三维分析框架,结合需求端驱动因素与区域发展特征,对市场格局进行系统剖析。
市场规模:整体扩张与细分赛道分化
2024年全球医疗AI市场规模已形成多维度统计格局:综合行业报告显示,整体市场规模在192亿美元至497.1亿美元区间,其中精准医疗AI细分领域达23.3亿美元,外科机器人市场约115亿美元[1][2][3]。细分市场中,生成式AI(GenAI)表现尤为突出,2023年规模约20亿美元,预计2027年将飙升至220亿美元,而脑机接口医疗应用等前沿领域远期(2030-2040年)规模或达400亿至1450亿美元[4][5]。从长期预测看,2030年全球医疗AI市场有望突破1.5万亿美元,其中药物研发、影像诊断、健康管理三大板块占比超60%,2036-2037年整体市场规模或将达到4.57万亿至6.4万亿美元量级[3][6][7]。
增长速率:整体高增与细分市场差异显著
全球医疗AI市场整体保持高速增长,2024-2030年年复合增长率(CAGR)普遍在36.4%-45.5%区间,其中2024-2032年CAGR达44.0%,市场规模预计从290.1亿美元增至5041.7亿美元[7][8][9]。细分领域增长分化特征明显:生成式AI以85%的CAGR远超行业平均水平,显著高于金融(44%)和零售(38%)行业增速;精准医疗AI在2024-2029年CAGR为32.2%,预计从23.3亿美元增至91.8亿美元;而外科机器人市场增速相对稳健,2025年起CAGR约12%[1][2][10]。这种差异主要源于技术成熟度与应用场景渗透速度的不同,生成式AI因在临床文档生成、药物发现等领域的突破性应用实现爆发式增长。
区域格局:北美主导与亚太崛起的双极态势
从区域分布看,北美市场目前占据主导地位,2024年全球医疗AI市场份额达49.29%,主要得益于成熟的HCIT基础设施与高额研发投入[8]。欧洲则在精准医疗AI领域表现突出,成为预测期内增长最快的地区[2]。亚太地区(以中国、印度为核心)正成为全球增长引擎,预计到2037年市场规模将积累2.5万亿美元,其增长动力来自三方面:一是政策红利显著,各国政府密集出台AI医疗支持政策;二是医疗资源缺口催生技术替代需求,尤其在基层诊疗领域;三是人口结构与产业基础优势,包括庞大的老龄化人口、慢性病患者基数及快速发展的制药行业[3]。
需求端驱动方面,全球65岁以上人口占比已超14%,慢性病患者数量突破3亿,两者共同推高对早期疾病筛查、个性化治疗的需求[11]。这种需求与AI技术在医疗数据处理、临床决策支持等领域的能力形成共振,成为市场持续扩张的核心动力。麦肯锡研究显示,到2030年AI应用有望为美国医疗系统节省超3000亿美元成本,进一步验证技术商业化价值[7]。
中国市场特点
二、技术进展与创新突破
核心技术演进
算法与算力支撑
算法优化通过模型结构创新与效率提升,显著推动医疗AI的临床适用性与资源利用效率。在医疗影像分析领域,卷积神经网络(CNN)的优化技术展现出突出成效:采用深度可分离卷积替代传统卷积层使模型参数量减少70%以上,结合动态通道剪枝技术,在保持病灶识别准确率的前提下实现推理速度提升40%。以肺部CT图像分类任务为例,优化后的ResNet-50变体在维持98.3%召回率的同时,单张图像处理时间从2.1秒缩短至0.8秒,知识蒸馏技术进一步将教师模型的特征表征能力迁移至轻量化学生模型,为边缘计算设备提供实时诊断支持[13]。算法优化的综合效益还体现在临床决策效率提升,AI医生系统在门诊场景中输出诊断一致性达98%(医学专家间共识率约60%),认证AI系统平均误诊率6.3%,显著低于基层医疗人类医生的12.7%;通过综合效率值模型(综合效率值=(准确率×接诊量)/(单位成本×√误诊率))测算,认证AI系统综合效率值达217.6,远超三甲医院人类医生的82.3,印证了算法优化对医疗服务质量与成本控制的双重价值[14]。
算力集群的分层建设为医疗AI规模化落地提供基础设施支撑,形成从国家级枢纽到终端节点的全链条算力供给体系。国家级层面,基于“人工智能新基建”工程的医疗算力中心已具备万亿级参数医学大模型训练能力,可支撑电子病历、影像组学、基因组学等跨模态数据的深度融合[15]。区域级算力网络呈现“集中调度+分布式部署”特征,如广东省构建500P国产化人工智能算力平台,实现区域智算、通算资源的统一管理与高效调度,并配套40个高价值语料库及154项高质量数据集,支持医疗机构通过数据交易所完成健康医疗数据产品的资产凭证与知识产权“双登记”[16]。在医疗机构层面,垂直算力网络建设成效显著:东莞通过“三级医院边缘智算设备+社卫中心轻量化算力节点”的架构,实现急诊影像实时分析与慢性病管理等场景的差异化算力适配,政府全额承担基层AI诊断工具的算力成本,三甲医院研发场景按实际消耗补贴50%,有效降低医疗AI落地门槛[17]。硬件技术进步进一步强化算力支撑能力,英伟达、AMD等企业新一代AI芯片实现算力提升10倍、成本下降50%,量子计算初步商用使复杂模型训练时间从数月缩短至几天,为医疗大模型的快速迭代提供可能[18]。
数据治理技术通过本地化部署与授权机制创新,在保障隐私安全的前提下促进医疗数据价值释放。DeepSeek大模型采用本地化部署模式,医疗数据无需上传云端即可在医院或企业内部完成封闭训练,有效规避传统开源模型的数据外训与云端接入风险,烟台毓璜顶医院基于该模式构建的智能网络安全运营平台,实现每天超1000万条日志的本地化分析,误报率降低76%,90%常见网络安全事件可在3分钟内自动处置[19][20]。授权数据处理机制推动高质量医疗数据汇聚,医渡科技核心算法引擎YiduCore累计处理60亿份经授权医疗记录,沉淀上万种疾病的理解洞察,专病库覆盖超过90个病种,产出20个专病领域数据集[21]。尽管当前医疗数据仍面临标准化不足的挑战(2021年三级医院医疗大数据应用率不足20%,二级医院不足5%),但通过行业可信数据空间建设与高质量数据集上架(如广东省卫生健康数据中台首批上架154项数据集),数据多源异构、标准体系不健全等问题正逐步缓解,为医疗AI模型训练提供更可靠的数据基础[16][22]。
三、应用场景与临床实践
临床诊疗核心场景
基于阿里云“成熟度-潜力”矩阵分析,临床诊疗核心场景呈现显著的场景分化特征。其中,影像诊断与药物研发凭借“高成熟度+高潜力”属性成为当前AI医疗的核心突破领域。在影像诊断领域,AI技术已实现高准确率与清晰商业化路径的双重优势,医学影像AI产品商业化率达90%,如推想医疗肺部CT AI辅助诊断系统、汇医慧影“CT肺结节辅助诊断系统”可在30秒内完成超500层CT影像判读,敏感性超过普通医生水平[10][23]。宋江典团队的视觉大语言模型进一步实现病变区域精准分割与动态风险评估,能以标准放射学报告语言输出随访过程中的病变变化,并实时调整癌变概率评估[24]。国家医保局将AI医学影像诊断技术(肺结节、乳腺癌、眼底病变筛查)纳入支付范围后,其临床价值进一步凸显,读片速度可达人工的20倍,基层医疗机构误诊率从18%降至7%[12]。
药物研发领域同样展现“双高”特征,AI技术通过生成式模型与多模态数据整合显著缩短研发周期。英矽智能生成式AI平台将抗体研发周期压缩10倍,实现四项药物授权合作,总金额超15亿美元;AI驱动的药物研发整体可缩短30%-50%的研发周期,商业化路径已通过临床试验验证,如医渡科技利用大数据+大模型技术打造智能筛选系统,肿瘤类项目平均节省88.5%人工筛查成本[5][25]。
相比之下,个性化治疗与健康管理仍处于“高潜力+低成熟度”阶段,核心瓶颈集中于数据整合与患者依从性。个性化治疗需整合多源异构数据(如基因、临床症状、生活习惯),但数据碎片化问题突出,例如退伍军人事务医疗中AI分析PTSD需结合服役经历、症状、基因数据,却面临跨系统数据互通障碍[26]。健康管理领域虽可通过AI生成定制化慢病方案,但患者依从性不足制约效果,如深圳三甲医院引入的DeepSeek智能问诊系统中,60岁以上患者使用比例不足18%,过半需他人协助操作[27]。
“AI+医生”协同模式成为突破技术落地瓶颈的关键路径,其临床价值已在多场景得到验证。北京儿童医院“AI儿科医生”首次应用于儿童罕见病MDT会诊,与15位专家同时得出相似诊断结论,明确患儿为常染色体显性颅骨干骺端发育不全[28]。南方医院AI智能总检大模型将单份报告生成时间从20分钟缩短至5分钟,漏诊率与误诊率分别降至0.03%和0.01%,上线两个月内完成16万人次报告智能总检,主检建议采纳率超92%[29]。医渡科技AI中台在30多家三甲医院部署应用,2025年2月至6月辅助医生累计服务患者达2.6万人次,实现肿瘤专科医院诊疗多场景突破性落地[21]。福建中医药大学附属人民医院通过DeepSeek R1大模型接入电子病历系统,医生可实时获取智能助手的分析思路和参考结果,体检系统则实现智能诊断与历史检查结果比对[30]。此类协同模式不仅提升诊断效率与准确性,更通过“AI辅助-医生决策”的分工优化医疗资源配置,为基层医疗与复杂疾病诊疗提供高效解决方案。
公共卫生与基层医疗
人工智能在公共卫生领域已形成“监测-预警-响应”全链条赋能体系。在监测环节,AI技术通过自动化收集分析多源数据实现精准识别,如同济医院“基于多点触发机制的大型医院重大突发公共卫生事件主动监测预警系统”,利用AI对临床数据进行自动化分析,识别传染病爆发前的关键指标[31];安徽省疾控中心“基于5G+人工智能技术的重大突发公共卫生事件智能预警与响应系统”建立六类症候群监测,可实时捕捉异常数据[32]。预警层面,AI通过构建预测模型实现风险前瞻,例如上海推行的“疾控大脑”整合病原基因序列分析等数据,可对传染病传播风险进行动态预测[33];包头市固阳县通过县域居民电子健康档案构建“健康预警网”,上线首月即捕捉3起聚集性腹泻事件并触发传染病预警[34]。响应阶段,AI辅助提升处置效率,如安徽省疾控系统通过预警信号确认11起阳性事件,为快速响应提供决策支持[32]。
基层医疗AI渗透率提升显著,2025年预计超过50%,但区域发展不均衡问题突出。以上海某三甲医院智能影像系统日均处理3000例检查为例,对比云南某乡镇卫生院AI终端每月仅激活27次,反映出数据质量、设备利用率及医生接受度等现实障碍[35]。解决方案聚焦“大医院技术下沉+基层场景适配”双路径:技术下沉方面,讯飞医疗“一体两翼”框架实现基层常见病全覆盖,华西医院与润达医疗联合研发的“睿兵Agent”聚焦消化领域,通过解决AI幻觉问题提升诊断可信度[5][10];南方医院计划2026年前将AI智能总检大模型覆盖全国100家基层医疗机构,辅助筛查甲状腺结节恶性风险等复杂病例[29]。场景适配层面,政策推动医保优先覆盖县域基层医疗机构,AI辅助诊断技术使基层误诊率从18%降至7%,其中包头固阳县布鲁氏菌病误诊率从30%降至12%,急性心梗预警准确率达78%[12][34]。
慢病管理领域,AI与可穿戴设备协同构建“数据监测-风险预警-干预管理”闭环。东莞试点研发AI驱动的糖尿病足监测手环,通过持续生理指标采集实现异常预警[17];医联集团整合居家监测设备IOT数据与临床数据,建立多维度动态健康档案,提供个性化慢病管理方案[36]。谷医堂动态健康监测平台针对糖尿病、高血压等慢病,通过数据分析实现早期风险预警,形成覆盖家庭、企业、医疗机构的三位一体健康管理网络[37]。北京亦庄试点部署慢性病智能预警系统,结合居家安全监护网络,为基层慢病管理提供技术支撑[38]。此类协同模式有效延伸了慢病管理的时空边界,提升了基层患者的健康管理效能。
特殊领域创新应用
在传统医学赋能方面,人工智能技术正深刻推动中医药的现代化发展。中国中医科学院广安门医院构建的“广医·岐智”大模型,以70年名老中医经验为基础,整合407万临床病例数据,形成包含9类1400万条记录的中医临床知识库,开发智能导诊、预问诊等智慧服务功能,实现中医诊疗经验的系统化传承与规模化应用[39]。上海地区通过推动人工智能与中医药深度融合,已形成智慧中医诊疗系统(涵盖问诊平台、疗效评价模型及名老中医数字化传承)和智慧中药药事服务(包括中药制剂疗效总结与中药饮片智能化管理)两大创新方向[33]。临床实践中,AI脉诊仪在社区医院的应用显示出显著效能,上海AI诊所数据表明,其对高血压、糖尿病的复诊效率提升3倍,患者满意度达91.7%,且与老中医诊断一致性高达88%,同时能多检出潜在风险因素,体现AI对中医诊疗流程的优化与能力延伸[40]。
康复医疗领域,人工智能技术通过创新治疗模式与体验优化,有效提升患者依从性与康复效果。深圳市养老护理院引入的AI康复治疗机器人,可提供艾灸、推拿、超声波等多样化康复服务,治疗过程中通过播放音乐舒缓患者身心,并自动吸收艾灸气味以改善治疗环境;机器人借助AI算法实现穴位精准定位,结合患者症状通过万向臂开展个性化治疗,从生理与心理层面提升老年患者的接受度[41]。神经康复领域的突破更具里程碑意义,复旦大学科研团队完成的全球首例微创脑脊接口手术,通过AI实时解码脑电信号并转化为电刺激信号,为脊髓损伤患者搭建“神经旁路”实现运动功能重建,截至2025年3月已成功完成4例手术,患者术后均实现快速康复[4][42]。临床数据显示,接受脑脊接口技术治疗的完全截瘫患者不仅重新实现站立行走,其心理健康维度生活质量评分提升47%,社会功能维度提升62%,印证了AI驱动的康复技术在改善患者生理功能与生活质量方面的双重价值[43]。
军事医疗AI因战场环境特殊性,需满足数据稀缺、实时决策等核心需求,技术适配性聚焦小样本学习与抗干扰能力。美国国防部首席数字和人工智能办公室(CDAO)开展的众包AI红队测试(CAIRT)试点项目,针对军事医学LLM聊天机器人的临床笔记总结和医疗咨询两个用例,组织超200名参与者(含临床提供者与医疗分析师)比较三种LLM,发现超800个潜在漏洞和偏见,为国防部生成式AI政策制定提供关键数据支持,凸显战场医疗数据质量与模型鲁棒性的重要性[44]。技术应用层面,AI在军事远程医疗中实现多维度赋能:机器学习技术支持疾病预测与风险评估、智能诊断决策及远程监控反馈;深度学习技术优化资源分配、提升诊断准确度并构建决策支持系统;自然语言处理技术则用于患者信息采集、远程咨询支持及医疗数据挖掘[45]。此外,机器人技术在军事医疗中展现独特优势,可协助完成伤员识别、生理监测、手术干预及补给后送等任务,尤其在污染环境中具备抗干扰与持续作业能力,进一步扩展了战场医疗后送范围与救治效率[46]。
四、政策法规与监管环境
中国政策框架
中国医疗人工智能政策体系呈现“顶层设计与地方试点协同推进”的鲜明特点。在顶层设计层面,国家通过多项战略文件构建政策框架:《健康中国2030规划纲要》明确加快医疗健康领域数字化转型,推动AI技术深度应用,目标2025年AI覆盖80%以上三级医院[47];“十四五”规划将AI医疗列为战略方向,《关于进一步完善医疗卫生服务体系的意见》则要求加速AI在医疗领域的落地应用[48]。地方试点层面,各地结合实际探索差异化路径,如上海发布《上海市发展医学人工智能工作方案(2025—2027年)》,从创新策源、支撑平台、应用场景三方面推进AI医疗发展[33];深圳出台《AI诊疗管理办法》,明确AI诊断结论需经医生二次确认、重大治疗方案需人工复核的操作规范[27][49];商丘市构建“三链融合”智能监控体系,覆盖55.48%的定点医疗机构和40.77%的定点零售药店,实现医保基金全流程监管[50],形成“国家引导、地方创新”的政策实施格局。
场景化政策对行业发展的引导作用显著。国家发布《卫生健康行业人工智能应用场景参考指引》,细化84个应用场景,重点推动AI在基层医疗的落地[5][10][51]。地方层面进一步拓展场景覆盖,如上海方案提出打造临床医疗、中医药、公共卫生、医疗管理融合的全领域应用场景[33];北京市支持AI+病理、AI+医学影像等不少于10个场景的模型开发应用[52]。这些场景化政策通过明确技术应用边界和路径,引导企业聚焦临床需求,加速AI技术从实验室向医疗实践转化。
监管趋严与创新平衡的路径逐步清晰。在监管层面,政策重点强化责任认定与风险防控:《互联网诊疗监管细则(试行)》明确处方须由接诊医师本人开具,严禁AI自动生成处方,湖南、北京等地均出台类似规定[48];AI医疗器械审批体系不断完善,截至2023年7月,国家药监局已批准59款AI软件作为医疗设备,2024年三类证审批周期缩短33%,同时要求AI产品经过临床验证[47][48][51]。在创新激励方面,地方试点探索灵活机制,如深圳要求AI结论经医生二次确认,北京大学深圳医院对AI问诊记录标注“非最终诊断”,在保障医疗安全的同时为技术创新保留空间[49];数据要素市场化配置政策也为AI创新提供支撑,《“数据要素×”三年行动计划(2024—2026年)》提出有序释放个人健康数据价值[48]。
医保支付政策成为推动AI商业化的关键引擎。国家层面将AI服务逐步纳入医保体系,2025年医保目录首次新增12项AI诊疗服务,报销比例控制在50%至70%区间,要求纳入医保的技术必须通过国家药监局认证,并采用“效果挂钩”支付模式,若AI诊断准确率未达预设标准,医保支付比例将动态调整[12][48]。地方试点进一步探索支付创新:东莞将AI辅助诊断、慢性病管理等服务按单次成本30%-50%报销[17];上海早在2021年就将“人工智能辅助治疗技术”纳入医保乙类目录,覆盖前列腺癌根治术等4类手术[53];国家医保局在放射检查项目中设立“人工智能辅助”扩展项,明确AI作用限于辅助诊断或提高效率,防止额外增加患者负担[54]。这些政策显著降低患者负担,如肺结节AI筛查患者实际自付费用低于100元,较传统检查降幅明显,有效推动AI技术的商业化落地和规模化应用。
国际监管比较
全球医疗人工智能监管体系呈现多元化发展态势,不同地区基于政策目标与价值导向形成了差异化路径。美国、欧盟和中国作为核心区域,其监管策略在创新促进、伦理合规与场景落地维度差异显著,同时全球正逐步形成若干共性监管趋势。
欧盟以伦理合规与风险防控为核心,构建了严格的监管框架。2023年《人工智能法案》将AI辅助诊断、机器人手术等医疗应用归类为高风险系统,要求通过严格临床验证并满足合规性与透明度标准,强调AI系统的可解释性[47]。此外,欧盟已启动“神经权利法案”立法,规范神经调控技术的“修复”与“改造”边界,进一步强化伦理边界控制[43]。相关研究表明,欧盟监管政策聚焦安全性,通过严格准入与持续监控保障患者权益[55]。
美国侧重以灵活监管促进创新速度,强调风险可控下的技术转化。FDA 2023年《AI医疗设备监管框架》采用基于风险的分类监管,2024年推出加速审批通道,为低风险或创新型设备提供快速上市路径[47]。2025年1月发布的《使用人工智能支持药品和生物制品监管决策的考量》指南草案,提出“可信度”概念及“七步走”评估框架,重点关注模型风险(由影响和决策后果决定)与技术层面(数据和训练)的验证,明确不涵盖药物发现阶段及仅提升操作效率的应用,体现对创新与风险平衡的动态调整[56]。此外,美国通过数字健康创新行动计划(DHIAP)及软件预认证计划优化监管流程,提升适应性[57]。研究指出,美国政策注重透明性与可解释性,以明确技术标准降低创新壁垒[55]。
中国聚焦场景落地与产业协同,推动医疗AI在临床场景的规模化应用。《医疗AI监管政策的国际比较研究》显示,中国政策研究重点涉及法律地位界定、责任划分及新型监管体系构建,为技术从实验室走向实际医疗服务提供制度保障[55]。这种以场景为导向的思路,注重平衡技术创新与临床实用性。
全球医疗AI监管正呈现两大核心趋势。一是算法透明度与可解释性要求日益明确。欧盟《人工智能法案》将可解释性作为高风险系统的核心合规要件,美国FDA可信度评估框架强调模型训练数据与技术过程的透明化验证,反映国际社会对AI决策逻辑可追溯性的重视[47][56]。二是数据跨境流动与隐私保护规范逐步完善。加拿大通过《隐私法》与《个人信息保护与电子文件法》(PIPEDA)强化个人数据保护,全球范围内对医疗数据跨境流动的合规性要求持续提升,推动建立数据安全与流通效率相平衡的规则[57]。
总体而言,国际医疗AI监管在差异中逐步趋同,各国在患者安全与技术创新间寻求动态平衡,算法透明度与数据规范的全球化协调将成为未来监管合作的关键方向。
五、产业格局与企业竞争
中国市场主体
国际企业与跨国合作
国际医疗AI企业通过多元化技术输出路径推动全球市场渗透,核心策略包括平台化赋能、战略协作与资本整合。技术输出方面,英伟达推出Clara医疗AI平台,已吸引全球数百家企业和医院注册使用,形成规模化技术扩散效应[57];微软、谷歌、AWS等科技巨头直接提供标准化医疗AI解决方案,而Accenture与AWS合作开发负责任AI平台,则体现了通过生态协同完善技术落地能力[8]。此外,资本层面的技术整合活跃,如英伟达和辉瑞领投以色列AI制药初创公司CytoReason 8000万美元融资,加速创新技术的产业化应用[2][22]。学术界、产业界与政府合作构建的开源平台及云工具,则为本土企业提供了低成本技术接入渠道,进一步拓宽了国际技术的普惠路径[58]。
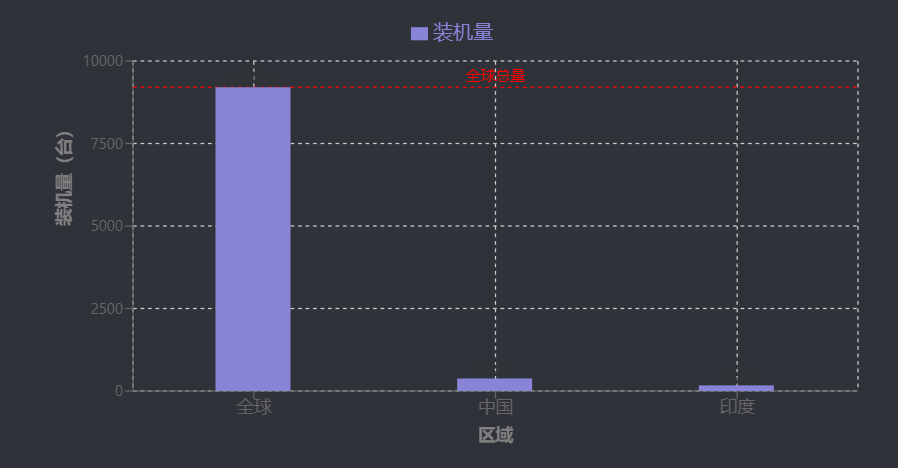
跨国合作在促进全球医疗资源普惠方面展现出显著价值,主要体现在技术下沉与公共卫生响应优化两大维度。针对医疗资源匮乏地区,美国数字健康企业Akido Labs将6000万美元B轮融资用于扩大ScopeAI平台在社区的部署,直接提升基层医疗服务能力[59]。在技术差距缩小方面,美国谷歌、IBM与中国华为、百度合作优化医学影像领域CT、MRI深度学习算法,推动核心技术标准的协同发展;全球多国在疫情防控中共享数据和AI模型,使公共卫生响应速度得到系统性提升[5][60]。医疗设备领域,达芬奇手术机器人2024年全球装机量达9203台,其中中国超380台、印度170多台,西门子Healthineers的AI-powered Luminos Q.namix平台提升放射科效率40%,均通过技术扩散缩小了区域医疗服务能力差距[5][61]。
中国企业出海策略呈现本土化适配与场景化渗透特征,“先试用后购买”模式与SaaS化服务成为打开新兴市场的关键路径。兰丁智能通过参与美国、欧洲、非洲等国际病理年会,以“先试用后购买”策略在越南、巴西、摩洛哥等国实现落地,其在巴西的临床验证显示AI系统阳性检出率与人工验证准确率达95%,并与巴基斯坦合作构建AI云平台开展远程诊断[62]。汇医慧影则依托SaaS化服务的可复制性,将AI抗疫解决方案推广至东南亚(泰国、马来西亚)、南美洲(厄瓜多尔)等20多个国家的50余所医院,形成标准化技术输出与本地化服务结合的拓展模式[23]。
六、挑战、伦理与风险
技术与数据挑战
医疗人工智能的发展面临严峻的技术与数据挑战,其中数据互通壁垒是核心瓶颈之一。其根源主要在于标准不统一与利益博弈:医疗数据在流通、共享、存储、管理等环节尚未形成统一标准,导致数据多源异构难以汇集,63%的医疗机构存在数据接口不兼容问题,数据标准化采集至今仍是行业痛点[19][22][35]。同时,机构间的数据孤岛现象显著,某跨国药企肺癌早筛模型因无法获取完整诊疗数据,准确率较美国同类产品低15个百分点,反映出数据共享中的利益博弈问题[35]。针对这一问题,当前解决方案包括推进区域医疗数据平台建设、普及联邦学习技术(如通过联邦学习+区块链保障跨机构协作中的数据所有权和隐私安全),以及建立数据贡献度评估机制与异常节点监测体系以避免模型偏移,同时推广《医疗健康行业大模型基础设施标准》促进数据互通,部分实践案例(如中国坪山医院的三级脱敏机制)已验证其可行性[13][63]。
算法偏见对医疗公平性构成严重威胁,直接影响不同群体的医疗可及性与服务质量。研究显示,AI诊断系统在深肤色人群中乳腺癌检出率低18%,反映出训练数据集中种族代表性不足导致的诊断偏差[63]。此外,老年群体面临物理层(生物特征样本不足、方言识别率低)、认知层(模糊表达、算法推荐导致数字迷失)的技术排斥,进一步加剧了医疗服务的不公平性,而通用开源模型(如LLaMA 2)在生物医疗领域的幻觉问题(约占测试样本的32%),可能对特定人群的诊断准确性造成二次伤害[64][65]。
算力与成本制约是中小企业参与医疗AI创新的主要障碍。AI医疗诊断辅助系统的训练成本高昂,涵盖数据采集(需保证准确性与完整性)、专业人员标注、高性能计算设备支持及硬件维护升级等环节,而训练一个大型AI模型的成本超千万美元,能源消耗相当于数百个家庭一年的用电量,且能耗随技术升级呈指数级增长[66][67]。在融资形势严峻的背景下,中国医疗AI企业普遍面临现金流压力,难以承担高额的算力与数据成本,导致技术研发与应用普及受限[68]。
此外,技术与数据挑战还体现在数据质量与安全风险。医疗数据碎片化、非标准化问题突出,2021年我国三级医院医疗大数据应用率不足20%,二级医院不足5%,临床数据研究开展比例仅五分之一[22]。数据安全事件频发,2023年国内医疗行业泄露数据达9亿条,数据泄露平均成本达977万美元,面临数据劫持、网络钓鱼、勒索攻击等多重风险[69]。算法层面,基于深度学习的AI模型存在“黑箱”属性,缺乏决策透明性与可解释性,且AI幻觉(如编造医学名词和参考文献)难以避免,可能危及患者生命安全[24][63]。这些问题共同构成了医疗人工智能技术落地与规模化应用的主要障碍。
伦理与监管风险
医疗人工智能的快速发展在带来技术革新的同时,也引发了一系列伦理困境与监管挑战,对技术落地与临床实践构成潜在风险。伦理层面,责任划分不清是核心矛盾之一。AI系统并非独立的医疗行为主体,缺乏处方权且无法承担法律责任,导致医疗事故发生后的责任追溯与赔偿机制难以有效运行。例如,当AI自动生成处方或诊断建议与临床医生判断冲突时(如老年患者林先生遭遇“AI建议新药但医生因肝功能问题反对”的情况),责任归属的模糊性可能直接引发医患纠纷。此外,AI技术对传统医疗模式的冲击也加剧了伦理争议,如AI中医的兴起引发守旧派对“机器替代人类医生直觉与经验”的担忧,国家中医药管理局因此明确规定AI不得单独出具诊断结论,以维护医疗质量与安全。
算法的公平性、透明性与敏感领域伦理规范同样构成严峻挑战。医疗大模型可能因训练数据偏差导致输出结果存在偏见,或因文化敏感性缺失引发伦理风险,例如提供违反宗教禁忌的饮食建议。在临终关怀、生殖医学等特殊领域,算法决策可能触及伦理红线,需建立强制人工复核机制;医疗机构伦理委员会的全生命周期审查机制尚未普及,进一步放大了技术滥用风险。此外,AI“幻觉”问题(如生成不准确医疗信息)以及数据不兼容导致的区域适配性不足(如欠发达地区因数据差异难以通过AI改善健康),也凸显了技术普惠与伦理包容性之间的失衡。
患者信任度不足是制约AI医疗落地的关键因素。杜克大学研究显示,在医疗服务中披露AI使用后,患者满意度较人类医生单独服务下降0.13分,较未披露AI使用场景下降0.09分,反映知情权与信任度之间的矛盾。老年群体表现尤为突出:深圳AI问诊系统中60岁以上患者使用率不足18%,超七成需现场志愿者协助,且存在“退出即清空输入”等操作障碍;长江商学院调研指出,“重度AI替代担忧者”的抑郁比例高达34.13%,老年患者对AI技术的焦虑感显著高于其他群体。信任危机还体现在临床决策冲突中,当AI建议与医生判断不一致时(如AI推荐新药但医生因患者个体差异否决),患者易对技术产生质疑,甚至误解AI结论为“最终诊断”,需医疗机构通过标注“非最终诊断”等方式防范风险。
监管滞后性与技术创新速度之间的矛盾进一步加剧了风险。当前AI医疗监管体系仍处于探索阶段,大模型应用规范、数据管理标准及医疗责任划分等核心问题尚未形成统一框架。算法的快速迭代与冗长的审批周期形成鲜明对比,例如医疗大模型的持续优化可能导致已获批版本与实际应用版本存在差异,增加合规风险。尽管部分领域已出台监管措施(如AI中医需医生二次确认),但面对神经调控技术中“修复”与“改造”的伦理边界界定、抗菌素耐药性防控中个体治疗与集体利益的平衡(跨国调查显示仅33.3%-54.0%受访者支持标准化方案)等复杂问题,现有监管手段仍显不足,亟需构建动态适配的治理体系以平衡创新与安全。
商业化与可持续性
七、患者接受度与社会影响
患者态度与使用行为
本研究构建“技术-过程-结果”三维接受度模型,系统分析患者对医疗人工智能的态度差异及使用行为特征。基于“三维四阶”信任度量化模型,技术可信度、过程感知度与结果满意度共同构成患者接受度的核心维度,其中技术可信度强调诊断准确率偏差值≤0.08及算法透明度评分≥85/100,过程感知度关注医患沟通时间占比≥40%与决策参与度指数7:3,结果满意度则以诊疗方案依从率≥92%和纠纷发生率≤0.3‰为关键指标[63][70]。动态权重分配机制显示,急诊场景下技术可信度权重高达0.6,而慢病管理更侧重过程感知度(权重0.55),反映不同医疗场景下患者需求的差异化[63][70]。
老年患者的抵触因素与适老化改造效果呈现显著对比。调研显示,60岁以上患者AI使用率不足18%,超半数需现场志愿者协助,其抵触根源包括操作复杂性与传统医疗信任依赖[27][49]。具体而言,82%的老年人因看不懂电子屏、找不到功能键或不会使用自助机产生焦虑,65%曾因忘带医保卡或不会操作手机支付放弃就医,技术陌生感甚至导致“生活遥控器被剥夺”的无力感[71][72]。此外,老年人对AI健康信息的不信任源于对技术接受程度低、依赖传统医疗信息来源,以及对数据准确性和隐私泄露的担忧[72]。
适老化改造有效缓解了上述矛盾。深圳养老护理院的AI康复治疗机器人通过非接触式艾灸、理疗过程播放音乐及自动吸收气味等优化设计,获得老年患者“下次还要做膝盖理疗”的积极反馈,体现功能适老化与情感关怀的结合[41]。语音交互等技术优化使老年患者接受度显著提升,结合“三维四阶”模型中过程感知度的改善,推动适老化改造后老年用户对AI医疗工具的评价向“可沟通、可信任”方向转变,与真人治疗师的体验差距逐步缩小[73]。
患者对AI透明化的需求贯穿技术应用全流程。在技术可信度层面,患者要求明确披露诊断逻辑,如“协和·太初”大模型通过初筛结论可靠性验证(近两周500余条使用记录显示结论基本可靠)建立信任基础[74]。过程感知度方面,医患沟通中AI角色的透明化表述显著影响接受度,患者最倾向接受“此消息由医生在自动化工具的支持下撰写”的披露方式,而直接告知“AI生成”会导致满意度略有下降[75]。结果满意度维度,上海AI诊所试点显示,高血压、糖尿病复诊效率提升3倍的同时,需通过“动态权重分配”机制平衡技术效率与透明化需求,最终实现患者满意度91.7%的效果[40]。
总体而言,患者态度呈现年龄分层特征:年轻群体将AI问诊视为“医疗版高德地图”,47%的25-35岁用户首选AI进行慢病复诊[40];而老年群体的接受度提升依赖适老化改造与透明化机制的双重保障。三维模型的实践表明,技术优化(如语音交互)、过程透明(如算法逻辑解释)与结果可感知(如康复效果量化)的协同,是提升整体接受度的关键,当前AI医生首诊采纳率58%的现状提示需进一步强化“技术-过程-结果”的闭环优化[14][43]。
医疗资源普惠与社会公平
人工智能技术在推动医疗资源普惠化与促进社会公平方面展现出显著潜力,其核心价值体现在打破时空限制、优化资源配置及降低服务成本等多个维度。在偏远及基层地区,AI通过远程诊断、辅助决策工具及标准化服务模式,有效缩小了与优质医疗资源的差距。例如,“粤医智影”系统使基层患者无需长途跋涉即可获得精准诊断,如某案例中患者从辗转3小时到县城检查转变为乡镇就地完成,显著提升了医疗可及性[16]。汇医慧影AI医学影像解决方案在新疆等偏远地区的应用,直接弥补了基层阅片能力的不足[23];兰丁AI数字病理解决方案通过便携式智能扫描仪与云平台结合,无需依赖高水平病理医生即可实现远程诊断,为发展中国家医疗资源短缺问题提供了可行路径[19]。在基层医疗能力提升方面,AI辅助诊断工具显著降低了误诊率,如医保政策优先覆盖的基层医疗机构,其误诊率从18%降至7%[12];包头市固阳县的基层AI诊疗系统将急性心梗等疾病的诊疗流程从转诊至市区压缩至26分钟内完成,并针对地方高发疾病优化“专病模块”,实现“医生省时省力,老百姓省心省钱”的双重效益[34]。
AI技术还通过降低服务成本与优化流程进一步促进公平。DAMO PANDA模型结合平扫CT的筛查费用约200元,远低于传统胃肠镜、增强CT累计至少3000元的成本,大幅降低了普通人群的筛查门槛[76];国家医保智能核销系统将门诊报销周期从72小时缩短至2分18秒,住院报销从超半月优化为快速处理,新药纳入周期缩短至72小时,显著提升了创新药需求群体的服务可及性[77]。在资源共享层面,中国中医科学院广安门医院联合6家医联体单位成立“广医岐智大模型智能体联盟”,推动优质中医资源下沉,使基层医生能够借助AI“拥有”国医大师经验[39];谷医堂通过远程问诊与电子脉诊技术打破地域限制,让基层患者直接享受优质中医资源[37]。
然而,AI技术的普惠进程仍面临显著障碍,核心表现为医疗资源分配的不均衡与数字鸿沟。以上海三甲医院与云南乡镇卫生院为例,两地AI设备使用频率差异显著,反映出经济发达地区与欠发达地区在技术落地与实际应用层面的差距[35]。这种差距不仅体现在硬件配置上,还可能涉及数据共享机制、基层人员操作能力等隐性因素,如湖南大数据交易所虽通过区块链实现医疗健康数据“可用不可见”,但跨区域、跨机构的资源流动仍需进一步突破技术与机制壁垒[35]。
为引导AI资源下沉,政策层面已形成多维度支持体系。在医保与采购策略方面,医保政策优先覆盖县域基层医疗机构,直接推动AI辅助诊断技术在基层的普及[12];河南省通过“分层分类”采购策略(基础诊疗层、综合诊疗层、区域诊疗中心)更新CT设备,针对性提升基层影像检查能力[78]。在协同机制上,“大医院技术下沉+基层场景适配”模式成为主流,如讯飞医疗、华西医院与润达医疗的合作案例,通过人机协作提升基层医生诊疗能力,优化患者就诊路径[10]。数据基础设施建设方面,浙江234家医院接入统一数据平台,将跨院CT报告调取时间从15分钟缩短至9秒,为资源高效流动奠定基础[35]。这些政策与技术手段的结合,正在逐步推动AI从“技术赋能”向“公平普惠”转化,但其长期效果仍需关注基层人员培训、数据安全与区域协同等持续性问题。
| 指标类别 | 改进前 | 改进后 | 变化幅度 | 来源 |
|---|---|---|---|---|
| 诊断准确率 | 18%误诊率 | 7%误诊率 | ↓61% | [12] |
| 筛查成本 | 3000元(传统方式) | 200元(AI方式) | ↓93.3% | [76] |
| 医保核销效率 | [77] | |||
| ・门诊报销 | 72小时 | 2分18秒 | ↓99.95% | |
| ・住院报销 | 超半月(约360小时) | 快速处理 | - | |
| ・新药纳入 | 月均(约720小时) | 72小时 | ↓90% | |
| 数据调取时间 | 15分钟 | 9秒 | ↓99% | [35] |
| 急诊响应 | 转诊至市区 | ≤26分钟 | - | [34] |
八、未来趋势与展望
技术融合与创新方向
当前医疗人工智能技术正呈现多维度融合趋势,其中多模态数据实时解析成为推动预防医学发展的核心动力。预训练大模型通过整合文本、影像、基因等多源数据提升诊断精准度,元训练大模型则凭借跨任务泛化能力实现动态治疗方案调整,二者共同构建起覆盖“预防-诊断-治疗-康复”全流程的智能体系[79]。例如,达摩院探索将PANDA模型技术应用于多种癌症及慢性病检测,未来有望通过一次平扫CT完成多疾病筛查,体现了多模态融合在早期诊断中的潜力[76]。在中医领域,福建中医药大学附属人民医院计划基于DeepSeek大模型训练“中医智能辅助决策智能体”,将辨证思维结构化处理,为精准诊疗提供支持[30];谷医堂则通过区块链技术实现药材溯源,并构建线上线下融合的“五位一体”中医馆系统,推动传统医学与现代技术的深度整合[37]。此外,AI与XR技术的融合为康复医学提供了数字化转型样本,基层医疗大模型一体机(如卫美健康整合70B参数模型的硬件设备)的部署则加速了智能医疗向基层渗透,形成“数据+知识”混合驱动的技术创新路径[80][81]。
前沿技术的临床转化正逐步突破传统医疗边界。脑机接口技术方面,加福民团队分阶段推进脑脊接口临床转化,开发植入式系统(针对重症患者)与非植入式穿戴设备(针对轻症患者),预计5-10年实现规模化普及,目标使脊髓损伤患者重获行走能力[43][82]。南方医院计划2025年底前将AI智能总检大模型接入脑机接口及代谢组学技术,实现阿尔茨海默病、肿瘤等疾病的超早期筛查,进一步拓展了该技术的应用场景[29]。在手术领域,AI实时指导已成为高难度手术的重要辅助手段,预计2025年顶级医院50%的复杂手术(如CTO导丝通过)将采用AI精准指导技术,而机器视觉、类脑芯片等军工技术的民用转化则为手术机器人提供了多模态感知与决策支持[83][84]。数字孪生技术方面,个人健康孪生体通过整合基因组、穿戴设备及电子病历数据,可预测未来5年健康风险并提供干预方案,成为动态疾病管理的新型工具[5]。
AI技术正深刻重构医疗服务范式,推动从“被动治疗”向“主动预测”转型。生成式AI通过构建动态疾病预测模型,已实现诊疗流程的根本性转变——从“被动响应”转向“主动预测”[10]。例如,AI帮助下阿尔茨海默病的五年预测准确率达80%以上,南方医院的超早期筛查系统及“AI健康管家”虚拟形象(提供7×24小时咨询)进一步验证了主动预防的可行性[19][29]。在服务模式上,分级诊疗中枢体系逐步形成:社区AI可处理70%常见病,三甲专家聚焦疑难重症;2025-2030年AI预计承担60%标准化门诊工作,使医生资源更集中于复杂病例处理[14]。全流程智慧医疗生态(如昭通市中医医院覆盖诊前、诊中、诊后的智能系统)与“预防-诊疗-康复”闭环(通过AI+5G+区块链技术构建)的形成,则标志着医疗服务从单点突破迈向全链条智能化[85][86]。未来,随着生成式AI向核心决策系统演进及自动化医学发现技术(如大模型提出靶点假设并由机器人实验室验证)的成熟,医疗行业有望实现从“人力密集型”向“智能驱动型”的价值创造模式转变[15]。
政策与产业生态演进
医疗人工智能领域的政策走向正经历从“创新鼓励”向“规范发展”的战略性转变。这一转变体现在监管体系的完善、法律法规的细化以及安全框架的构建等多个层面。政策层面将进一步完善AI医疗设备监管体系,重点解决医学伦理与隐私保护问题,同时持续推动AI技术在基层医疗的渗透,预计2025年基层医院AI渗透率将超过50%[51][60]。为实现规范发展,需强化医疗数据安全防护,通过加密算法、访问控制、安全存储、数据管理规章及人员培训等措施,结合军事保密规定与民用数据安全标准(如HIPAA)构建保护体系,统筹安全与发展,依法依规管理医疗数据[46][69]。此外,完善AI技术相关法律法规,明确大模型应用规范、数据管理及医疗责任划分,加强监管机制建设,已成为政策制定的核心方向[81]。
产业协同对医疗AI技术落地的加速作用显著,其核心在于构建数据驱动的运营体系与全链条成果转化机制。地方实践中,东莞计划构建医疗垂直算力网络,并定向发放医疗专用算力券,在2025年5000万元总额中划拨30%专项支持基层与三甲医院算力需求,为技术落地提供基础设施支撑[17]。同时,概念验证与成果转化链条的贯通成为关键,如朝阳区重点推进“AI+精准诊疗”区域品牌建设,推动基础研究、应用研究与概念验证融合发展,缩短从学术研究到商业产品的转化周期[87]。产学研用协同生态的完善进一步加速技术落地,例如上海通过工作方案打造医学人工智能技术创新、应用示范和产业发展高地,推动全领域应用场景落地,促进从基础研究到产业落地的全链条体系构建[33][88]。
全球医疗AI标准统一呈现加速趋势,其基础在于跨区域合作机制与数据互认框架的构建。各国政府出台的政策加速了AI技术在医疗领域的全球整合与创新,国际合作项目不断增长,医疗AI技术及产品向亚洲等新兴市场辐射[47][57]。数据互联互通是标准统一的关键支撑,随着认知智能技术成熟,跨区域数据互认需求日益凸显,推动产业生态向更规范、健康、有序的方向发展[89]。此外,公共与私营部门的协同治理体系成为重要保障,公共部门需平衡AI风险与收益,加强监管;私营部门则需维护证据、道德、公平、安全和隐私等标准,共同推动可持续创新应用生态的形成[90]。这一趋势为WHO等国际组织推动全球数据互认与标准统一奠定了实践基础。
商业化路径探索
医疗人工智能的商业化进程正围绕高成熟度场景突破、基层市场渗透及基础设施化演进三大方向展开。在商业化突破口方面,当前聚焦于医学影像诊断与药物研发两大高潜力领域。其中,医学影像AI产品商业化率已达90%,成为技术落地最为成熟的场景之一;AI药物研发通过多源数据整合与算法优化,可缩短30%-50%研发周期,显著提升药企研发效率,推动形成“AI技术提供方与药企风险共担、收益分成”的合作模式[5][10]。健康管理领域则探索出“硬件+订阅服务”的创新路径,例如东莞结合潮玩产业开发的智能健康监测设备,通过硬件销售与健康数据订阅服务结合,构建可持续的消费级商业模式[17]。此外,商业模式正从单一产品销售向“服务+数据”转型,包括与保险公司合作开发数字疗法保险产品、提供个性化健康管理订阅服务等,推动AI医疗向场景化、生态化方向发展[22][91]。
基层医疗市场成为商业化拓展的核心增量空间,政策与支付体系改革共同驱动渗透加速。县域医共体作为基层医疗服务的关键载体,其AI渗透率目标设定为50%,商业化路径涵盖G端采购(政府付费)、医院直接买单、企业与医疗机构生态共建及商业保险合作等多元模式[81]。医保支付改革进一步降低技术普及门槛,例如部分地区将AI医疗服务纳入报销范围,报销比例达50%-70%,直接减轻患者经济负担,提升基层医疗机构采购意愿[12]。同时,针对基层医疗资源不足的痛点,AI系统通过整合电子健康记录、影像数据等多源信息,支持从辅助诊断向主动治疗规划演进,例如在心脏病学中早期识别高风险患者,为基层提供同质化诊疗能力支撑,进一步释放市场潜力[92]。
从长期发展看,AI医疗正逐步向“基础设施”演进,预计2030年将覆盖80%医疗场景。2025年作为商业化关键转折点,技术已从诊断支持向治疗规划、健康管理等全流程渗透,例如肿瘤学中AI基于肿瘤特征推荐化疗方案以提高缓解率,心脏病学中通过影像分析实现早期风险识别[92]。未来五年,随着数据互通壁垒逐步破除(如清华大学紫荆智康Agent Hospital多智能体协同模型)、跨学科协作深化及成本分析体系完善,AI医疗将从垂直场景向综合服务延伸[5][93]。结合政策推动(如县域医共体渗透率目标)与技术成熟度提升,预计到2030年,AI将深度融入预防、诊断、治疗、康复等核心医疗场景,成为支撑医疗体系高效运转的关键基础设施[5]。
商业化进程中需同步解决可持续性与普惠性平衡问题。当前探索的创新定价模式包括纳入DRG/DIP支付体系、数字医疗券、分层定价及服务付费等,例如海南省明确数字疗法收费政策后,已吸引商业保险开发配套产品,而重庆市汇人健康等企业通过循证医学证据与合规定价加速产品落地[35][78][91]。同时,通过开源平台降低创新门槛(如医疗大模型开源生态)、结合临床监督(如Therabot模式)及构建数据驱动的运营体系,将进一步推动AI医疗在商业化与医疗价值间的协调发展[5][58]。
